Úvod
V posledních letech vyvíjejí různé výzkumné ústavy a podniky regenerativní lékařské produkty*1 s cílem usnadnit rozšíření regenerativní medicíny. Protože kontrola kvality je pro regenerativní lékařské výrobky zásadní, vydala Agentura pro léčiva a zdravotnické prostředky (PMDA) různé materiály[1][2]. Testovací systém EZ-LX Zátěžová buňka 10 N Zkušební zařízení Zkušební zařízení pro tahové zkoušky kultivované epidermis Tabulka 2 Informace o vzorku Rozměry 50 mm × 100 mm který provádí recenze. Ačkoli vydané materiály požadují kromě biologických hodnocení i dynamická hodnocení, neobsahují popis konkrétních metod hodnocení. Dynamické hodnocení bylo provedeno po transplantaci pigmentových buněk sítnice odvozených z iPS buněk. Typy Tloušťka menší než 100 μm Mléčná membrána Kultivovaná epidermis A Kultivovaná epidermis B Tabulka 3 Podmínky zkoušky epiteliálních buněčných listů, ale metoda hodnocení byla pouze kvalitativní, spočívala pouze v kontrole poškození v době přípravy štěpu.[3] Kvantitativní hodnocení však bude pravděpodobně nutné u buněčných listů[5], které vyžadují mechanickou pevnost, jako jsou listy kultivované kůže[4] a listy z myokardiálních buněk. Kromě toho je možné, že na rozdíl od současných regenerativních zdravotnických výrobků využívajících autologní buňky bude u regenerativních zdravotnických výrobků využívajících alogenní buňky[6], u nichž se očekává, že se v budoucnu stanou hlavním proudem, nutné dodržovat specifikační testy založené na kvantitativních normách kvality. V tomto výzkumu byly provedeny tahové zkoušky s použitím kultivované epidermis, která je regenerativním zdravotnickým výrobkem, a mléčné membrány imitující kultivovanou epidermis (odebrané z povrchu horkého mléka) jako příklad kvantitativního hodnocení mechanických vlastností materiálu.*1 Regenerativní lékařské výrobky jsou výrobky vytvořené zpracováním lidských nebo zvířecích buněk pro rekonstrukci, opravu nebo formování tělesných struktur a funkcí nebo pro léčbu či prevenci nemocí.
Systém měření
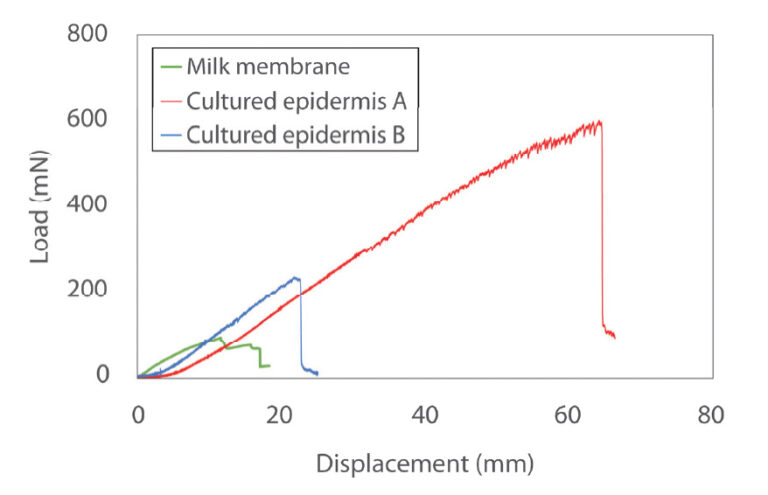
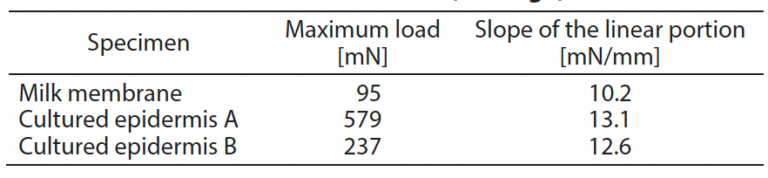
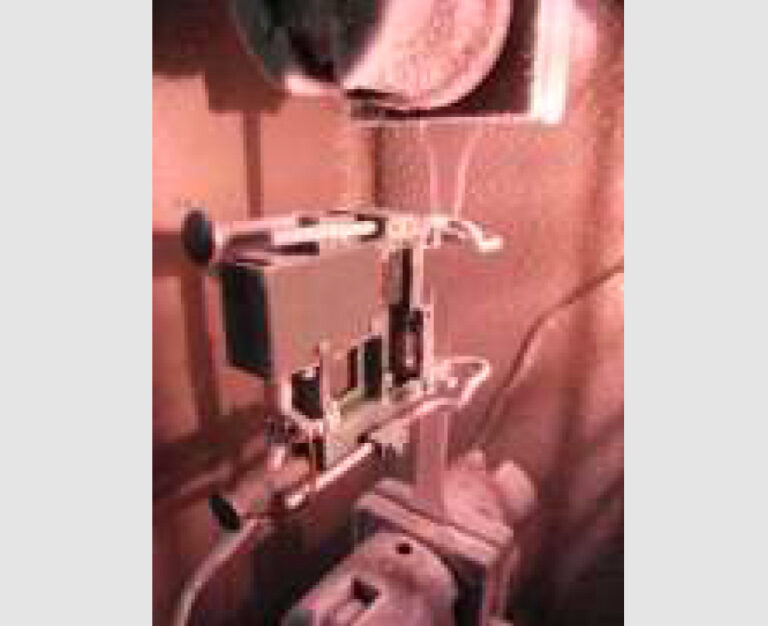
Tabulka 1 a tabulka 2 uvádějí složení systému a a informace o vzorcích. Na obr. 1 je znázorněn kultivovaný vzorek epidermis. Testy byly provedeny s použitím mléčné membrány imitující kultivovanou epidermis (fiktivní vzorek) a dvou typů vzorků pro výzkumné účely. kultivované epidermis (A a B)*2 s různou pevností. vyrobených stejnou metodou jako autologní vzorky. kultivované epidermis JACE®. Tloušťka kultivované epidermis byla menší než 100 μm a tloušťka struktura vzorků se skládala z několika vrstev. epidermálních buněk. Vzorky byly pružné a udržované ve vlhku namáčením v konzervačním roztoku. Vzorky proto musely být rychle upevněny a změřeny během tahových zkoušek, aby se zachovaly jejich vlastnosti. vlhkost. Na obr. 2 je obrázek zkoušky. Válcový houby jsou použity pro upevnění. Obalením vzorku kolem těchto houbiček, lze vzorky během zkoušky držet bez jejich poškození. Tabulka 3 ukazuje zkoušku podmínky. Rychlost zkoušky byla nastavena na nízkou rychlost v rámci v rozsahu rychlostí, při nichž vzorky zůstávají vlhké.*2 Poskytla společnost Japan Tissue Engineering Co., Ltd.